
dla pacjentów i lekarzy
Rak gruczołowy żołądka - opracowanie dla lekarzy
Spis treści:
1 Epidemiologia
2 Czynniki ryzyka
3 Objawy
4 Patomorfologia
5 Badania diagnostyczne w raku żołądka
5.1 Gastroskopia
5.2 Badanie fizykalne
5.3 Badania radiologiczne
5.4 Badania USG
5.5 Endosonografia (EUS)
5.6 Tomografia komputerowa i rezonans magnetyczny
5.7 Laparoskopia diagnostyczna
5.8 Markery nowotworowe
6 Klasyfikacja i ocena stopnia zaawansowania raka żołądka
6.1 Klasyfikacja TNM raka żołądka
6.2 Stopień zaawansowania (ang. staging) raka zołądka
7 Leczenie raka żołądka
7.1 Szczegółowe zasady w poszczególnych stopniach zaawansowania
7.2 Rak zaawansowany miejscowo naciekający okoliczne narządy
7.3 Dootrzewnowa chemioterapia perfuzyjna w hypertermii
7.4 Leczenie uogólnionego raka żołądka
7.5 Chemioterapia i radioterapia
7.6 Schematy chemioterapii
8 Rokowanie, obserwacja po leczeniu
9 Inne materiały na temat raka żołądka
Epidemiologia raka żołądka
Liczba zachorowań na nowotwory układu pokarmowego w Polsce, w 2017 roku, wynosiła ponad 31900, a liczba zgonów przekroczyła 28000. W większości przypadków guzy przewodu pokarmowego są nowotworami źle rokującymi, co znajduje odzwierciedlenie w niewielkiej różnicy między liczbą zachorowań i zgonów w poszczególnych latach obserwacji.
Zachorowalność na raka gruczołowego żołądka w Polsce w roku 2017 wynosiła 3261 nowych zachorowań wśród mężczyzn (3,96% wszystkich nowo rozpoznanych nowotworów złośliwych) oraz 1953 zachorowań u kobiet (2,37%). Ilość zgonów w roku 2017 wynosiła odpowiednio 3156 wśród mężczyzn (5,78% zgonów z powodu choroby nowotworowej) oraz 1777 zgonów u kobiet (3,94%). Mężczyźni chorują więc prawie dwukrotnie częściej.
Pod względem zachorowalności, nowotwory żołądka plasują się na 7 miejscu u mężczyzn i poza pierwszą 10 u kobiet wśród wszystkich diagnozowanych nowotworów złośliwych. Pod względem umieralności nowotwory żołądka zajmują 4 miejsce u mężczyzn oraz 7 u kobiet.
Mimo, że w Polsce, podobnie jak na całym świecie, obserwuje się systematycznie zmniejszającą się zachorowalność, jak i umieralność z powodu nowotworów żołądka, nadal wartość tych współczynników w naszym kraju należy do najwyższych w Europie.
Czynniki ryzyka raka żołądka
Do wzrostu ryzyka rozwoju raka żołądka, powstałego z przyczyn sporadycznych, w istotny sposób przyczyniają się warunki środowiskowe, w tym dieta, złożona z produktów sztucznie konserwowanych, solonych i wędzonych oraz tych będących źródłem nitrozoamin.
Jak w przypadku większości nowotworów, palenie papierosów oraz spożywanie alkoholi, szczególnie wysokoprocentowych, w nadmiernych ilościach może zwiększać ryzyko rozwoju choroby. Rola tytoniu w onkogenezie została potwierdzona w przypadku wielu typów histologicznych nowotworów złośliwych. Palenie prowadzi do obniżenia poziomu witaminy C, która przeciwdziała procesowi karcinogenezy (transformacji zdrowej tkanki w nowotworową). Substancje zawarte w dymie tytoniowym poprzez bezpośrednie działanie drażniące mięśniówkę żołądka i sploty nerwowe podśluzówkowe, powodują niewydolność mechanizmów sterujących perystaltyką. Skutkiem tego może być zarzucanie treści dwunastniczej do żołądka, nieżyt błony śluzowej i jej żółciowe zapalenie, które mogą mieć wpływ na powstanie przemian nowotworowych w komórkach gruczołowych, począwszy od zapalnego zaniku błony śluzowej, poprzez metaplazję, dysplazję i transformację złośliwą. Poza wymienionymi, uwagę zwracają zakażenia, w tym bakteryjne. Infekcja pałeczką Helicobacter pylori jest czynnikiem ryzyka raka żołądka typu jelitowego. Największy wpływ na nowotworzenie mają szczepy bakterii wykazujące ekspresję genów kodujących białko cagA, cytotoksyny vacA s1 lub vacA m1.
Więcej informacji w opracowaniu:
Zakażenie błony śluzowej żołądka bakterią Helicobacter pylori
U podłoża specyficznych zmian genetycznych (m.in. polimorfizmów cytokin prozapalnych) leży rozwój raka żołądka w grupie młodszych pacjentów, przed 45 rokiem życia (mutacja genu E-kadheryny — CDH1). Inne defekty genetyczne, związane z rodzinnymi zespołami większej podatności na nowotwory różnych lokalizacji także zwiększają prawdopodobieństwo zachorowania.
W chorobach autoimmunologicznych, których idealnym przykładem jest tutaj niedokrwistość megaloblastyczna Addisona-Biermera, obserwuje się nawet 3-6 krotny wzrost ryzyka wystąpienia raka żołądka. W zespole tym dochodzi do autoimmunologicznego zapalenia błony śluzowej żołądka z zanikiem na skutek działania przeciwciał skierowanych przeciwko komórkom okładzinowym błony śluzowej żołądka.
Choroba Menetriera (przerostowe zapalenie żołądka) jest rzadko spotykaną jednostką o nieznanej etiologii. Występuje 4 razy częściej u mężczyzn, najprawdopodobniej wiąże się z nadmierną ekspresją czynnika wzrostu TGF-α, który doprowadza do rozrostu komórek dołeczkowych oraz spadku liczby komórek okładzinowych żołądka. W następstwie, obserwuje się zwiększone wytwarzanie śluzu oraz utratę białka. Zmiany makroskopowe obserwowane w gastroskopii polegają na nadmiernym zgrubieniu fałdów części lub rzadziej całego żołądka. Objawy kliniczne to typowy ból nadbrzusza pojawiającym się tuż po posiłku, w obserwacjach odległych spadek apetytu, dyspepsję, utratę masy ciała i objawy niedożywienia, towarzyszące obniżeniu poziomu białka i albumin w osoczu krwi (hipoalbuminemia), do których należą obrzęki i przesięki do jam ciała. Uznaje się, że choroba Menetrier’a jest stanem przedrakowym, choć statystyczne zagrożenie wystąpieniem raka na podłożu tej choroby nie jest znane.
Do czynników ryzyka przemiany złośliwej należą także polipy umiejscowione w błonie śluzowej żołądka. Ryzyko przemiany złośliwej związane jest istotnie z charakterem histopatologicznym, wielkością i morfologią guza. Polipy hiperplastyczne, polipy z gruczołów żołądkowych właściwych wiążą się z mniejszym ryzykiem, podczas gdy polipy gruczolakowe mogą aż u 40% chorych przejść przemianę złośliwą. Szczególną uwagę należy zwrócić na polipy kosmkowe, o średnicy większej niż 2 cm, szybko rosnące, na szerokiej podstawie (tzw. polip siedzący). Rozwój raka we wcześniej istniejącym wrzodzie trawiennym występuje statystycznie rzadko, w mniej niż 1% przypadków. Należy zwrócić uwagę, iż owrzodzenia nowotworowe mogą częściowo goić się pod wpływem leczenia farmakologicznego, ale częściej proces ten jest utrudniony - niegojące się zmiany wymagają pilnej diagnostyki histologicznej (kontrolnej gastroskopii z pobraniem licznych wycinków i oceną histopatologiczną).
Rak żołądka częściej występuje u osób z grupa krwi A. Obciążenia dziedziczne, uwarunkowania genetyczne, występowanie nowotworów żołądka w najbliższej rodzinie, są wskazaniem do ścisłej, częstej kontroli i weryfikacji wszelkich nowych, niepokojących objawów. Zdrowy tryb życia, unikanie używek, pokarmy bogate w witaminę C, inne antyoksydanty, świeże owoce i warzywa wydają się mieć wpływ ochraniający.
Objawy raka żołądka
Rak żołądka, we wczesnych stadiach zaawansowania zazwyczaj nie daje objawów na tyle charakterystycznych, by od razu nasunąć podejrzenie procesu nowotworowego. Liczne nieskuteczne próby leczenia zachowawczego (objawowego) zgłaszanych dolegliwości skłaniają do poszerzenia diagnostyki o endoskopię i badania obrazowe, na ich podstawie stawiane jest rozpoznanie.
Objawy, mogące sugerować patologię w obrębie żołądka to tzw. dyspepsja - przewlekłe bóle brzucha zwłaszcza o stałym charakterze, zlokalizowane w nadbrzuszu, nasilające się po posiłku, a zmniejszające na czczo, nieustępujące po lekach zobojętniających, szybkie poposiłkowe uczucie pełności, odbijania, nudności i wymioty, brak łaknienia czy zgaga. Zwracanie pokarmów (nie mylić z wymiotami) występuje w przypadku guza wpustu zamykającego przejście z przełyku do żołądka. Poza tym, przy długo trwającym procesie pojawiają się objawy niedokrwistości, związane z krwawieniem z guza, jak i zajęciem błony śluzowej żołądka, spadkiem produkcji i niedoborem czynnika wewnętrznego i co za tym idzie, zmniejszonym wchłanianiem witaminy B12 (niedokrwistość megaloblastyczna).
Dysfagia, termin określający utrudnione przechodzenie pokarmu z jamy ustnej przez przełyk do żołądka może towarzyszyć nowotworom o lokalizacji okołowpustowej. Krwawienie z guza manifestuje się pod postacią smolistych stolców bądź wymiotów z domieszką świeżej (wpust) lub hemolizowanej krwi (tzw. wymioty fusowate - okolica trzonu żołądka i odźwiernikowa).
Utrata masy ciała i postępujące wyniszczenie związane są zarówno z utrudnieniem w przyjmowaniu pokarmów, jak i kacheksją nowotworową w zaawansowanej postaci choroby. Stany podgorączkowe, poty nocne mogą towarzyszyć w późniejszym okresie choroby, może dochodzić także do rozwoju zespołów paraneoplastycznych. Gdy dochodzi do wtórnego zajęcia węzłów chłonnych i narządów odległych obserwujemy objaw Troisiera (powiększony węzeł Virchowa w dole nadobojczykowym lewym) oraz powiększenie wątroby z towarzyszącym wodobrzuszem.
Patomorfologia raka żołądka
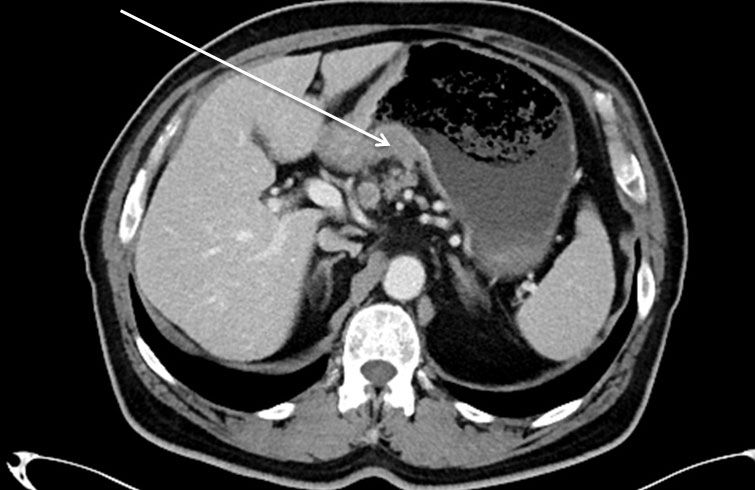
Najczęściej występującym nowotworem złośliwym żołądka jest gruczolakorak (rak gruczołowy żołądka). Znacznie rzadziej występują chłoniaki, nowotwory podścieliskowe przewodu pokarmowego (GIST- gastrointestinal stromal tumors), mięsaki (sarcoma) i nowotwory neuroendokrynne (NET- neuroendocrine tumors).
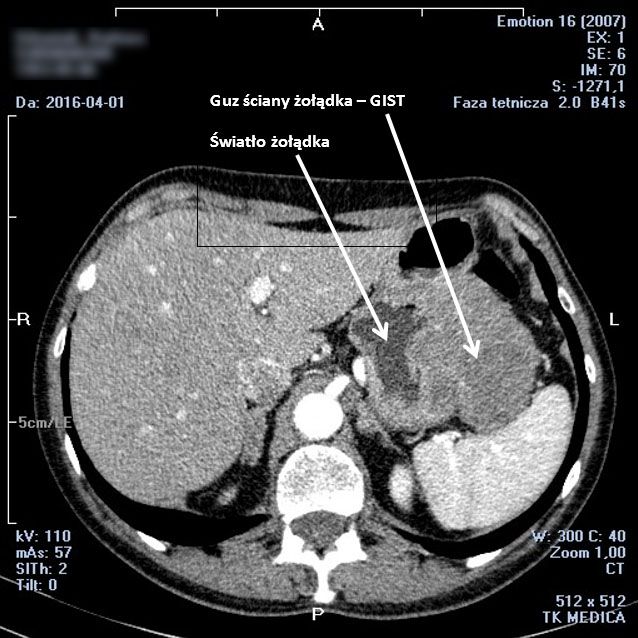
Fot. - Nowotwór podścieliskowy przewodu pokarmowego (GIST - ang. gastrointestinal stromal tumors) w obrazie badania TK (tomografia komputerowa)
Klasyfikacja Lauréna, uwzględniająca morfologię komórek i sposób naciekania, wyróżnia dwa podstawowe typy raka żołądka - typ jelitowy i typ rozlany. Klasyfikacja ma znaczenie rokownicze oraz jest przydatna przy podejmowaniu decyzji klinicznych dotyczących zakresu resekcji żołądka.
1. Typ jelitowy, morfologicznie podobny do błony śluzowej jelita (w strukturze przeważa budowa gruczołowa z komórkami przypominającymi cylindryczne komórki jelitowe oraz obecność komórek kubkowych wytwarzających kwaśne mukopolisacharydy). Towarzyszy mu zwykle zanikowe zapalenie błony śluzowej wraz z metaplazją jelitową. Typ ten charakteryzuje się lepszym rokowaniem, a zmniejszenie zachorowalności na raka żołądka obserwowane na przełomie ostatnich lat dotyczy głównie typu jelitowego;
2. Typ rozlany — cechujący się obecnością pojedynczych komórek lub małych gniazd raka o niewielkiej kohezji. Rozrasta się śródściennie z rozproszonymi komórkami nowotworowymi, nie tworząc wyraźnych granic. Ze względu na wysoki stopień złośliwości charakteryzuje się gorszym rokowaniem.
Rozpoznanie choroby powinno być potwierdzone w badaniu histologicznym (wycinki pobrane podczas gastroskopii lub zwiadowczej laparotomii) obejmującym typ histologiczny nowotworu oraz stan receptorów HER2 (immunohistochemicznie określenie nadekspresji (HER2 +++), a w przypadkach granicznej wartości (HER2++) dodatkowo ocena amplifikacji genu HER2 metodą FISH). Dodatni stan HER2 stwierdza się najczęściej w raku żołądka typu jelitowego zlokalizowanym we wpuście żołądka lub połączeniu przełykowo-żołądkowym.
Badania diagnostyczne w raku żołądka
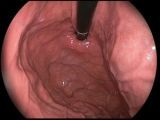
Gastroskopia
Gastroskopia jest najlepszą i najczęściej wybieraną metodą na początku ścieżki diagnostycznej przy podejrzeniu raka żołądka. Stwarza możliwość wstępnej oceny przełyku, okolicy wpustu żołądka i pozostałych jego odcinków, a także części poziomej dwunastnicy umiejscowionej za odźwiernikiem. Poza tym kleszczykami gastroskopu można pobrać do badania histologicznego materiał z guza - decydujący o rozpoznaniu, zidentyfikować nosicielstwo Helicobacter pylori (celem wdrożenia ewentualnego leczenia eradykacyjnego). W trakcie badania istotne jest pobranie jak najwięcej, co najmniej 6, wycinków, w tym przynajmniej jeden z dna owrzodzenia (usuwając tkanki martwicze), tak, aby pobrany materiał był jak najbardziej reprezentatywny.
Trudności diagnostyczne sprawia postać śródścienna (linitis plastica), która bywa niezauważona podczas wykonywania endoskopii, gdyż błona śluzowa może nie być zmieniona nowotworowo. Należy pamiętać o tych przypadkach, gdyż brak tkanki nowotworowej w pobranych wycinkach opóźnia diagnozę i odwleka w czasie możliwość podjęcia leczenia chirurgicznego. Ta postać nowotworu może być spowodowana śródściennym rakiem gruczołowym lub chłoniakiem. W badaniu radiologicznym z kontrastem żołądek daje obraz „sztywnej rury”, bez fal perystaltycznych w części zajętej przez naciek śródścienny.
Rozpoznanie wczesnego raka żołądka wymaga perfekcyjnej techniki badania, doświadczenia i odpowiedniego sprzętu. W przypadku każdego zaważonego wrzodu żołądka uznanego za trawienny należy pobierać wycinki oraz kontrolować zagojenie po wdrożonym leczeniu zachowawczym. Długo i z trudem gojące się owrzodzenia powinny nasuwać podejrzenie procesu rozrostowego.
W Polsce nie prowadzi się badań przesiewowych w kierunku raka żołądka. W krajach o wysokim ryzyku zachorowania (np. Japonia) jest prowadzony program przesiewowych badań z użyciem metod radiologicznych i endoskopowych. Identyfikacja grup zwiększonego ryzyka obejmuje test na obecność Helicobacter pylori oraz oznaczanie frakcji pepsynogenu. Zwiększone ryzyko towarzyszy osobom z zanikowym zapaleniem żołądka, niedokrwistością spowodowaną niedoborem witaminy B12, po przebytej resekcji żołądka, po usunięciu gruczolaka żołądka, z zachorowaniami na raka żołądka w rodzinie oraz członkom rodzin z zespołem Lyncha i rodzinną polipowatością gruczolakowatą.
Gastroskopia - przebieg badania, jak się przygotować do badania
jest to badanie wykonywane przy podejrzeniu zmian w obrębie przełyku, żołądka i początkowej części dwunastnicy. Do badania należy być na czczo, przynajmniej kilka godzin (3-6), tak aby nie było zalegania treści pokarmowej w żołądku, którą trudno usunąć za pomocą gastroskopu. Zalecenia dotyczące wziernikowania górnego odcinka przewodu pokarmowego przedstawiono poniżej:
- W dniu badania pacjent musi być na czczo. Dopuszczalne jest picie wody, ale na godzinę przed badaniem powinien zaprzestać picia płynów.
- Osoby z chorobami wymagającymi stałego, regularnego przyjmowania leków (np. nadciśnienie tętnicze, choroby serca, padaczka i inne): w dniu badania należy zażyć poranną dawkę leku popijając niewielką ilością wody.
- Osoby chorujące na cukrzycę powinny skonsultować z lekarzem prowadzącym sposób przygotowania do badania oraz poinformować lekarza wykonującego badanie.
- Osoby przyjmujące leki obniżające krzepliwość krwi (np. acenokumarol, sintrom, ticlid, plavix lub aspirynę i inne) powinny poinformować lekarza wykonującego badanie).
Badanie polega na włożeniu giętkiego endoskopu przez usta do gardła i dalej do przełyku i żołądka. Ze względu na silny odruch wymiotny przy dotknięciu tylnej ściany gardła przed badaniem lekarz znieczula gardło środkiem znieczulającym w aerozolu. Trzeba pamiętać, że odruch połykania zostaje upośledzony na kilka godzin i próba połykania po badaniu endoskopowym płynów lub pokarmów może spowodować zachłyśnięcie dróg oddechowych!
Jeśli pacjent jest bardzo pobudzony i boi się badania, należy zapytać lekarza, czy mógłby podać wcześniej leki uspokajające. W trakcie badania endoskopowego pobiera się szczypczykami wycinki do badania histopatologicznego. Z miejsc, z których pobrano wycinki może dojść do niewielkiego krwawienia, o czym lekarz powinien poinformować. Czasami podanie dużej ilości powietrza w trakcie badania może spowodować wzdęcia i uczucie dyskomfortu w brzuchu oraz odbijania.
Opracowanie na podstawie informacji ze strony: www.endo-gastro.pl, dzięki uprzejmości dr med. Jerzego Wegnera, specjalisty gastroenterologa
Badanie fizykalne
Badanie fizykalne chorego jest istotnym uzupełnieniem badań obrazowych. Stwierdzenie masy guza w nadbrzuszu lub śródbrzuszu wyczuwalnej przez powłoki podczas badania fizykalnego, z bolesnością w nadbrzuszu, nasuwa podejrzenie mocno zaawansowanego miejscowo procesu chorobowego. Zaobserwowane cechy świadczące o niedokrwistości (bladość powłok, ogólne osłabienie) mogą sugerować konieczność suplementacji z racji istniejących niedoborów bądź zaopatrzenie preparatami krwiopochodnymi. Zażółcenie powłok nasuwa podejrzenie zajęcia procesem chorobowym wątroby lub dróg żółciowych. Badanie nadobojczyków może wykazać obecność powiększonych, przerzutowych węzłów chłonnych (węzeł Virchowa).
U każdego chorego należy zwrócić uwagę na stopień odżywienia oraz cechy wyniszczenia (patrz: kliniczne cechy niedożywienia). Badania krwi istotne, poza podstawową morfologią, to te świadczące o zaawansowaniu procesów katabolicznych: poziom białka całkowitego, albumin, profil odporności.
Badanie radiologiczne
Badanie radiologiczne żołądka z podaniem doustnie kontrastu (najczęściej preparat zawierający baryt) pozwala na uwidocznienie zarysów ścian żołądka wraz z guzem i określenie jego stanu czynnościowego (upośledzenie perystaltyki – skurczów żołądka – w przypadku rozległych guzów nowotworowych i typu szerzącego się śródściennie (linitis plastica).
Badanie radiologiczne nie jest alternatywą dla gastroskopii, gdyż pozwala jedynie na wysunięcie podejrzenia nowotworowej patologii, a nie pełną diagnostykę. Jednak w przypadku linitis plastica badanie radiologiczne jest bardzo istotne - w wycinkach może nie być tkanki nowotworowej, zaś o konieczności wykonania zabiegu operacyjnego decyduje całość obrazu klinicznego i stwierdzenie cech rozległego nacieku w badaniu radiologicznym.
Planując badanie endoskopowe i radiologiczne z użyciem kontrastu (baryt), należy pamiętać o tym, że wcześniej wykonane badanie radiologiczne może uniemozliwić wykonanie endoskopii ze względu na zaleganie kontrastu. (Patrz: "Diagnoza - rak! I co dalej?" Poradnik dla pacjenta)
Ultrasonografia
Ultrasonografia pozwala na uwidocznienie powiększonych węzłów chłonnych (węzły większe niż 10 mm są podejrzane o obecność przerzutów), pozwala na ocenę obecności zmian wtórnych w wątrobie (czułość badania tym większa im większe są przerzuty), ocenę stanu i poszerzenia wewnątrzwątrobowych dróg żółciowych - w przypadku ucisku zewnątrzwątrobowych dróg żółciowych przez przerzutowe węzły chłonne wnęki wątroby bądź bezpośredni ucisk guza na głowę trzustki.
Badanie ma ograniczoną wartość ze względu na możliwą obecność gazów w jelitach, które zaburzają przechodzenie fal ultradźwiękowych.
Endosonografia (EUS) - ultrasonografia endoskopowa
Endosonografia (EUS), czyli ultrasonografia endoskopowa ma porównywalną skuteczność diagnostyczną z innymi badaniami obrazowymi; jedynie we wczesnych postaciach nowotworu charakteryzuje się większą przydatnością. Jest to badanie wykonywane głowicą umiejscowioną na końcówce endoskopu, przyłożoną bezpośrednio do ściany żołądka, pozwala na dokładną ocenę grubości nacieku nowotworowego oraz uwidacznia węzły chłonne wielkości ponad 5 mm w sąsiedztwie guza. Ma zastosowanie we wczesnym raku żołądka.
Tomografia komputerowa (TK) i magnetyczny rezonans jądrowy (NMR)
Tomografia komputerowa (TK) i magnetyczny rezonans jądrowy (NMR) to badania z wyboru wykonywane nie tylko celem oceny stopnia zaawansowania miejscowego guza, w stosunku do innych narządów, naciekania naczyń i innych struktur, ale również identyfikacji przerzutów odległych (staging).
W przypadku braku potwierdzenia cech nieoperacyjności badaniami obrazowymi, chory przygotowywany jest do zabiegu laparotomii diagnostycznej lub leczniczej z gastrektomią, zaś ostateczna decyzja o operacyjności raka żołądka należy do doświadczonego chirurga w trakcie procedury.
Laparoskopia diagnostyczna
Laparoskopia diagnostyczna nie jest badaniem wykonywanym rutynowo, aczkolwiek pozwala na ocenę obecności przerzutów do wątroby, do otrzewnej oraz naciekania okolicznych narządów. Badanie jest wykorzystywane w kwalifikacji chorych do chemioterapii indukcyjnej lub zabiegu dootrzewnowej chemioterapii perfuzyjnej wraz z resekcją żołądka (więcej na stronie: www.hipec.pl)
Markery nowotworowe
Markery nowotworowe to specyficzne substancje obecne we krwi, moczu bądź w wycinkach z tkanek pacjenta, których identyfikacja zaliczana jest do istotnych testów w onkologii. Badanie ich rodzaju oraz stężenia ułatwia postawienie diagnozy, ocenę ryzyka i długookresowe monitorowanie stanu zdrowia chorego. Swoistość i czułość markerów jest bardzo różna; stosunkowo mała ilość została uznana za w pełni wiarygodne i pewne źródło wiedzy o zaawansowaniu choroby nowotworowej, prawidłowe stężenie markera nie wyklucza obecności nowotworu (zmienność osobnicza poziomu wyjściowego), umiarkowane podwyższenie markerów (szczególnie pochodzenia tkankowego) występuje w chorobach nienowotworowych. Reasumując, oznaczanie markerów ma znaczenie pomocnicze i nie może zastąpić pełnego badania klinicznego. Na wysuwanie właściwych wniosków pozwalają jedynie pomiary wykonywane seryjnie w określonych odstępach czasu i w tych samych warunkach testowania.
W przypadku raka żołądka najczęściej ocenia się poziom CEA (antygen rakowo-płodowy) i CA 19-9. Ich podwyższony poziom występuje częściej w zaawansowanych postaciach raka żołądka i sugeruje gorsze rokowanie. Nie mniej jednak pomiary markerów są istotne, gdy w trakcie stawiania diagnozy obserwowano wzrost poziomów, ich normalizację po leczeniu i ponowne wysokie wartości w toku obserwacji pooperacyjnej - świadczące wówczas o wznowie choroby.
Klasyfikacja i ocena stopnia zaawansowania raka żołądka
Klasyfikacja TNM raka żołądka (8. edycja UICC)
Klasyfikacja TNM służy ocenie zaawansowania klinicznego nowotworów złośliwych. W przypadku raka żołądka klasyfikacja ta odnosi się do raków powstałych w obrębie żołądka, czyli w odległości większej niż 5 cm od połączenia przełykowo-żołądkowego lub w obrębie 5 cm od połączenia przełykowo-żołądkowego i nieszerzących się na przełyk.
| T (tumor) - guz pierwotny nowotworu | |
|---|---|
| Tx | nie można ocenić guza pierwotnego |
| T0 | nie stwierdza się guza pierwotnego |
| Tis | rak przedinwazyjny (in-situ) – rak nie naciekający blaszki właściwej błony śluzowej, dysplazja wysokiego stopnia |
| T1 | guz nacieka blaszkę właściwą lub blaszkę mięśniową błony śluzowej lub warstwę podśluzową |
| T1a | guz nacieka blaszkę właściwą lub blaszkę mięśniową błony śluzowej |
| T1b | guz nacieka warstwę podśluzową |
| T2 | guz nacieka warstwę mięśniową właściwą |
| T3 | guz nacieka warstwę podsurowicówkową |
| T4 | guz nacieka otrzewną trzewną lub sąsiednie struktury tkankowe |
| T4a | guz nacieka otrzewną trzewną |
| T4b | guz nacieka sąsiednie struktury tkankowe* |
| N (lymph nodes) - stan regionalnych węzłów chłonnych | |
|---|---|
| Nx | nie można ocenić regionalnych węzłów chłonnych |
| N0 | nie stwierdza się przerzutów w regionalnych węzłach chłonnych |
| N1 | przerzuty w 1–2 regionalnych węzłach chłonnych |
| N2 | przerzuty w 3–6 regionalnych węzłach chłonnych |
| N3 | przerzuty w 7 lub więcej regionalnych węzłach chłonnych |
| N3a | przerzuty w 7–15 regionalnych węzłach chłonnych |
| N3b | Przerzuty w 16 lub więcej regionalnych węzłach chłonnych |
| M (metastases) - przerzuty odległe | |
|---|---|
| M0 | nie stwierdza się obecności przerzutów odległych |
| M1 | występują przerzuty odległe, w tym przerzuty do otrzewnej, dodatnie badanie cytologiczne płynu z otrzewnej, przerzut do sieci większej nie stanowiący bezpośredniego nacieku guza pierwotnego |
*Sąsiednie struktury tkankowe: śledziona, okrężnica poprzeczna, wątroba, przepona, trzustka, powłoki jamy brzusznej (otrzewna ścienna), nerka, nadnercze, jelito cienkie. Także jeśli rak żołądka szerzy się przez ciągłość na więzadło żołądkowo-okrężnicze i sieć większą lub na więzadło żołądkowo-wątrobowe, bez przerywania otrzewnej trzewnej pokrywającej przez ciągłość
Regionalnymi węzłami chłonnymi dla żołądka są: węzły okołożołądkowe położone wzdłuż krzywizny mniejszej i większej (stacje nr 1–6; wg JGCA), węzły położone wzdłuż tętnicy żołądkowej lewej (7), tętnicy wątrobowej wspólnej (8), tętnicy śledzionowej (11), pnia trzewnego (9) oraz węzły wątrobowo-dwunastnicze (12).
Przerzuty w pozaregionalnych węzłach chłonnych, takich jak węzły chłonne zatrzustkowe (13), krezkowe (14, 15) i okołoaortalne (16), klasyfikowane są jako przerzuty odległe (M1).
Stopień zaawansowania (ang. staging) raka zołądka (8. edycja UICC)
| Stopień zaawansowania raka żołądka - ocena kliniczna (cTNM) | |
|---|---|
| Stopień 0 | Tis N0 M0 |
| Stopień I | T1,T2 N0 M0 |
| Stopień IIA | T1,T2 N1,N2,N3 M0 |
| Stopień IIB | T3,T4a N0 M0 |
| Stopień III | T3,T4a N1,N2,N3 M0 |
| Stopień IVA | T4b każdy N M0 |
| Stopień IVB | każdy T każdy N M1 |
| Stopień zaawansowania raka żołądka - ocena patologiczna (pTNM) | |
|---|---|
| Stopień 0 | Tis N0 M0 |
| Stopień IA | T1 N0 M0 |
| Stopień IB | T1 N1 M0 |
| T2 N0 M0 | |
| Stopień IIA | T1 N2 M0 |
| T2 N1 M0 | |
| T3 N0 M0 | |
| Stopień IIB | T1 N3a M0 |
| T2 N2 M0 | |
| T3 N1 M0 | |
| T4a N0 M0 | |
| Stopień IIIA | T2 N3a M0 |
| T3 N2 M0 | |
| T4a N1,N2 M0 | |
| T4b N0 M0 | |
| Stopień IIIB | T1,T2 N3b M0 |
| T3,T4a N3a M0 | |
| T4b N1,N2 M0 | |
| Stopień IIIC | T3,T4a N3b M0 |
| T4b N3a,N3b M0 | |
| Stopień IV | każdy T każdy N M1 |
Uwaga: ze względu na różne rokowanie w przypadku obecnych przerzutów do otrzewnej (peritonitis carcinomatosa), traktowanych w klasyfikacji TNM jako przerzuty odległe – tak jak przerzuty drogą krwi, np. do płuc, stosuje się w niektórych opracowaniach dodatkową klasyfikację:
| P - peritonitis carcinomatosa | |
|---|---|
| P0 | brak przerzutów do otrzewnej |
| P1 | obecne przerzuty do otrzewnej nie większe niż 0,5 cm |
| P2 | obecne przerzuty do otrzewnej wielkości 0,5 – 2,0 cm |
| P3 | obecne przerzuty do otrzewnej wielkości powyżej 2,0 cm |
Klasyfikacja ta istotna jest w momencie planowania procedury HIPEC.
Klasyfikacja Sugerbaker’a:
Do oceny zakresu obecności przerzutów do otrzewnej służy klasyfikacja Sugerbaker’a. Ocenia on wielkość guzków przerzutowych w poszczególnych umiejscowieniach otrzewnej ściennej w 13 regionach jamy otrzewnej. Każda zmiana jest klasyfikowana w skali 3 stopniowej. Tak więc w przypadku obecnych przerzutów do otrzewnej zakres zaawansowania według klasyfikacji Sugerbaker’a wynosi od 1 do 39 punktów. Im mniej punktów (mniejsze guzki i zakres ich obecności w regionach otrzewnej jamy brzusznej), tym lepsze wyniki leczenia za pomocą zabiegu dootrzewnowej chemioterapii w hipertermii (ang. HIPEC).
Przeczytaj więcej na temat dootrzewnowej chemioterapii w hipertermii (HIPEC) na stronach: Metody leczenia - HIPEC oraz www.hipec.pl
Klasyfikacja endoskopowa raka wczesnego (ograniczonego do błony śluzowej i podśluzowej):
I – guz wypukły, polipowata zmiana błony śluzowej
IIa – guz nieznacznie uwypuklony
IIb – guz płaski
IIc – guz zagłębiony
III – owrzodzenie błony śluzowej
Klasyfikacja endoskopowa raka miejscowo zaawansowanego według Borrmana:
I – pojedynczy polipowaty guz bez owrzodzenia
II – owrzodzenie o uniesionych, wyraźnie odgraniczonych brzegach
III – owrzodzenie o niewyraźnych, niezbyt dobrze odgraniczonych od błony bluzowej brzegach
IV – rozlany rak żołądka (linitis plastica), rozlegle naciekający ścianę, upośledzona perystaltyka (kurczenie się) żołądka
Klasyfikacja Goseki (podział oparty na zdolności do tworzenia struktur gruczołowych i ilości śluzu wewnątrz komórki):
Typ I - liczne, dobrze uformowane gruczoły, mała ilość śluzu w komórkach
Typ II - liczne gruczoły, duża ilość śluzu w komórkach
Typ III - słabo uformowane gruczoły, mała ilość śluzu w komórkach
Typ IV - słabo uformowane gruczoły, duża ilość śluzu w komórkach
Klasyfikacja według Laurena:
Najbardziej przydatna klinicznie jest klasyfikacja wg Laurena (wspomniana wcześniej, w sekcji patomorfologia), w której wyróżniamy 2 typy:
I – Typ jelitowy (ograniczony typ wzrostu)
II – Typ rozlany (rozlany typ wzrostu)
III – Typ mieszany (klinicznie traktowany jak typ rozlany)
Stopień złośliwości (grade) histologicznej raka gruczołowego żołądka:
Gx – brak możliwości oceny stopnia złośliwości
G1 – guz dobrze zróżnicowany
G2 – guz średnio zróżnicowany
G3 – guz słabo zróżnicowany
G4 – guz niezróżnicowany
Leczenie raka żołądka
Przygotowanie żywieniowe do leczenia chirurgicznego
Chorzy z nowotworami przewodu pokarmowego wykazują w wielu przypadkach cechy niedożywienia, wynikające zarówno z zaawansowania choroby (niedrożność, biegunka, wymioty) jak i zmian metabolicznych, których przyczyną jest stres związany z poważną chorobą.
Stan odżywienia jest jednym z czynników determinujących wybór metody leczenia. Zły stan odżywienia może skutkować niemożnością przeprowadzenia leczenia operacyjnego czy chemioterapii. Wpływa też bezpośrednio na wyniki wdrożonego leczenia, możliwość wystąpienia powikłań i dalsze rokowania.
Istotne jest, aby każdy pacjent był należycie przygotowany do leczenia, a zwłaszcza do zabiegu chirurgicznego. Chorzy w złym stanie odżywienia powinni otrzymać wsparcie żywieniowe przed zabiegiem (preparaty wysokobiałkowe, wysokokaloryczne). Leczenie żywieniowe powinno być nieodłączną częścią właściwego procesu leczniczego.
Więcej informacji w dziale Leczenie żywieniowe.
Siódme wydanie klasyfikacji TNM według UICC/AJCC z 2010 roku, a także nowa wersja japońskiej klasyfikacji raka żołądka i zaleceń leczniczych, Japanese Gastric Cancer Association (JGCA) (3. edycja z 2010 r.), zmieniają definicje limfadenektomii D1/D2, w zależności od rozległości resekcji żołądka. Zalecane jest wycięcie co najmniej 2/3 żołądka z limfadenektomią D2, która obejmuje stacje węzłów chłonnych 1, 2*, 3–7 (okołożołądkowe, D1) oraz 8, 9, 10*, 11 i 12 (*węzły chłonne okołowpustowe lewe i wnęki śledziony nie muszą być usuwane w czasie resekcji dalszej części żołądka).
Należy dążyć do tego, aby wynik badania histologicznego preparatu chirurgicznego po regionalnej limfadenektomii zawierał ocenę co najmniej 15 węzłów chłonnych.
Splenektomia nie jest zalecana. Wycięcie śledziony jest dopuszczalne w przypadku podejrzenia jej bezpośredniego naciekania przez nowotwór (przez ciągłość) lub zajęcia wnęki śledziony (pomijając okołooperacyjne przyczyny chirurgiczne). U chorych, u których przewiduje się pooperacyjną chemioradioterapię, obciążonych, z objawami niedożywienia i wymagających przedoperacyjnego leczenia żywieniowego, można rozważać jednoczasowe wykonanie jejunostomii odżywczej (mikroprzetoka do pierwszej pętli jelita czczego) - do dojelitowego podawania preparatów odżywczych).
Przedoperacyjna (neoadjuwantowa) chemioterapia niekiedy stosowana jest w rakach połączenia przełykowo-żołądkowego, natomiast jej zastosowanie w rakach żołądka jest przedmiotem badań klinicznych. Napromienianie paliatywne u chorych z guzem nieresekcyjnym jest uzasadnione wyłącznie w przypadkach objawowych niedokrwistości spowodowanych krwawieniem z guza.
U chorych na resekcyjnego raka żołądka lub raka połączenia przełykowo-żołądkowego okołooperacyjna chemioterapia (stosowana zarówno przed, jak i po zabiegu) pozwala uzyskać wydłużenie czasu przeżycia (całkowitego i wolnego od nawrotu choroby) w porównaniu z wyłącznym leczeniem operacyjnym.
Podobne obserwacje dotyczą uzupełniającej chemioradioterapii. Mimo że metoda ta została uznana za standardową w Stanach Zjednoczonych, w krajach europejskich zwykle wykorzystuje się ją u chorych po nieoptymalnej limfadenektomii (obejmującej < 15 węzłów chłonnych) lub po resekcji mikroskopowo nieradykalnej (R1).
Chemioterapia rozsianego raka żołądka wpływa zarówno na przedłużenie czasu przeżycia, jak i poprawę jakości życia chorych.
Leczenie — szczegółowe zasady w poszczególnych stopniach zaawansowania
Wczesne postacie raka (T1aN0; < 2 cm; G1) mogą być leczone metodami endoskopowymi za pomocą endoskopowej podśluzówkowej dyssekcji (ESD, endoscopic submucosal dissection).
U chorych na wczesnego raka żołądka (≤ T1bN0–1M0) zakres operacji można ograniczyć do częściowej resekcji żołądka oraz limfadenektomii D1+ (stacje węzłowe 1–7, 8, 9).
W krajach, w których dzięki badaniom przesiewowym (endoskopia) często rak żołądka jest wykrywany we wczesnym stopniu zaawansowania (np. Japonia) praktyką jest częściowe wycięcie ściany żołądka wraz z guzem, również za pomocą technik laparoskopowych. W tych przypadkach nie wykonuje się limfadenektomii, a coraz częściej oznacza się i usuwa do badania węzły wartownicze. Można to wykonać podając znacznik (barwnik, izotop) podsurowicówkowo, a następnie zidentyfikować węzły wartownicze bądź wizualnie (metoda barwnikowa) lub z użyciem ręcznego detektora promieniowania gamma (gamma-kamera). Możliwe jest także podanie znacznika podśluzówkowo za pomocą endoskopii, a następnie laparoskopowe oznaczenie węzła wartowniczego gamma-kamerą przeznaczoną do zabiegów laparoskopowych - celem wysłania do badania histopatologicznego. Identyfikacja węzła wartowniczego pozwala na wyselekcjonowanie pierwszego węzła na drodze naczyń chłonnych biegnących od guza w stronę regionalnego układu chłonnego. W przypadku braku obecności przerzutów w węźle wartowniczym nie wykonuje się pełnej limfadenektomii.
We wszystkich innych (wyższych) stopniach zaawansowania zaleca się wycięcie całkowite żołądka z limfadenektomią D2.
W przypadku guza o typie jelitowym według klasyfikacji Laurena (lepsze rokowanie), umiejscowionym w obwodowej, przedoddźwiernikowej części żołądka, można wykonać częściowe wycięcie tego narządu. W każdym innym przypadku (inne umiejscowienie, guz o typie rozlanym lub mieszanym) należy wykonać całkowite wycięcie żołądka.
Najczęstszym sposobem całkowitego wycięcia żołądka jest operacja sposobem Roux-en-Y. Polega ona na wycięciu żołądka, zamknięciu bliższej (odżołądkowej) części dwunastnicy, przecięciu pętli jelita cienkiego, zespoleniu z podprzeponową częścią przełyku (szwami pojedynczymi lub staplerem okrężnym).
W przypadku zabiegu radykalnego (wykonywanego z intencją wyleczenia) należy wyciąć regionalne węzły chłonne, w zakresie D2. W niektórych ośrodkach wykonuje się limfadenektomię D3, ale nie jest to postępowanie obowiązujące, zaś ilość powikłań związanych z rozszerzeniem zakresu wycięcia węzłów chłonnych jest znacząco większa.
W przypadku guzów umiejscowionych we wpuście oraz naciekających przełyk lub odnogi przepony, często konieczne jest otwarcie klatki piersiowej (thoracolaparotomia) i wycięcie dolnej części przełyku. Zespolenie przełykowo-jelitowe wykonywane jest wówczas w klatce piersiowej, szwami ręcznymi lub używając staplera okrężnego. Należy zwrócić dokładną uwagę na właściwe ukrwienie kikuta jelita i miejsca zespolenia - upośledzone ukrwienie, nawet niewielkie, brzeżne, może być przyczyną nieszczelności i poważnych powikłań (ropień opłucnowy, zapalenie śródpiersia tylnego).
W każdym przypadku zespoleń należy pamiętać o podstawowych zasadach, które gwarantują sukces zabiegu:
- dobre ukrwienie zespalanych tkanek
- brak napięcia miejsca zespolenia
- szerokie zespolenie, umożliwiające swobodne przechodzenie pokarmów i treści
- dokładna hemostaza
Doszczętność zabiegu operacyjnego określa się według stopnia R (residua – pozostałość, reszta):
R0 – brak pozostałości nowotworu, zarówno w postaci makroskopowej jak i mikroskopowej – zabieg radykalny
R1 – pozostawienie nowotworu w postaci mikroskopowej (np. obecność komórek nowotworowych w popłuczynach z jamy otrzewnej po zabiegu resekcyjnym w przypadku raka naciekającego błonę surowiczą (T3) lub naciekającego okoliczne narządy (T4); dodatnie marginesy w ocenie histopatologicznej)
R2 – pozostawienie tkanki nowotworowej widocznej makroskopowo (zabiegi paliatywne, cytoredukcyjne)
W przypadku stwierdzenia naciekania sąsiednich narządów usprawiedliwione są resekcje poszerzone o ich wycięcie. Rozszerzanie zakresu limfadenektomii o węzły chłonne okołoaortalne nie jest uzasadnione.
U chorych z cechą M1 w dobrym stanie ogólnym zalecane są chemioterapia lub chirurgia paliatywna, natomiast u chorych w złym stanie ogólnym rekomenduje się wyłącznie postępowanie objawowe.
Nie zaleca się paliatywnej resekcji żołądka, gdy u chorego nie występują objawy kliniczne.
Rak zaawansowany miejscowo naciekający okoliczne narządy
Naciekanie jelita grubego, ogona trzustki, brzegu wątroby, odnóg przepony, sieci większej czy otrzewnej ściennej nie powinno być przyczyną odstępowania od wykonania zabiegu resekcji żołądka z intencją wyleczenia, a w szczególności uznania nowotworu za nieoperacyjny. Niektórzy chorzy powinni być także (po wykonaniu zabiegu cytoredukcji) kwalifikowani do leczenia uzupełniającego za pomocą dootrzewnowej chemioterapii perfuzyjnej w podwyższonej temperaturze (HIPEC) lub chemioterapii systemowej. Wskazaniami do zastosowania HIPEC są obecność komórek nowotworowych w popłuczynach z jamy otrzewnej oraz obecność ograniczonych przerzutów do otrzewnej (w badaniu histopatologicznym pobranych zmian stwierdza się utkanie raka gruczołowego).
Ważne: do zabiegów HIPEC kwalifikują się ci chorzy, u których możliwe jest wykonanie całkowitej cytoredukcji guza. O kwalifikacji chorego do tak agresywnego leczenia decyduje stan ogólny i możliwość uzyskania spodziewanych korzyści leczniczych przy minimalnej ilości powikłań związanych z leczeniem.
Dootrzewnowa chemioterapia perfuzyjna w hipertermii (HIPEC)
U chorych, u których nie ma potwierdzonych badaniami radiologicznymi (rezonans magnetyczny, tomografia komputerowa, PET) przerzutów drogą krwi, lub są one niewielkie i mogą być leczone skutecznie innymi metodami (np. pojedynczy przerzut do płuca, przerzuty raka jelita grubego do wątroby do 3 ognisk), rokowanie w przypadku samych przerzutów do otrzewnej jest korzystniejsze, szczególnie, gdy wdroży się postępowanie według standardów procedury HIPEC. Wyniki leczenia są tym lepsze, im mniejszą powierzchnię otrzewnej zajmują.
Procedura (stosowana do leczenia przerzutów do otrzewnej raka jajnika, jelita grubego, raka żołądka, międzybłoniaka otrzewnej, śluzaka rzekomego otrzewnej) składa się z dwóch etapów: w pierwszym dąży się metodami chirurgicznymi do uzyskania całkowitej cytoredukcji - usunięcia masy guza wraz z przerzutowo zmienionymi tkankami i narządami. Ta część zabiegu jest bardzo trudna technicznie, długotrwała i mocno obciążająca chorego - stąd istotna jest dokładna i rzetelna kwalifikacja tych chorych, którzy z procedury odniosą jak największą korzyść.
Drugi etap procedury to ciągła perfuzja (płukanie) jamy otrzewnej roztworem cytostatyku podgrzanego do temperatury 42 stopni Celsjusza. Czas trwania perfuzji zależy od podanego leku przeciwnowotworowego i wynosi od 30 do 90 minut. Rodzaj chemioterapeutyku dostosowuje się do typu nowotworu pierwotnego i jego chemio wrażliwości - celem zapewnienia najwyższej skuteczności. Zastosowanie chemioterapii bezpośrednio na tkanki przebudowane nowotworowo pozwala podać maksymalne dawki cytostatyków i jednocześnie zminimalizować ich działania ogólnoustrojowe. Czas trwania całej procedury (zabieg cytoredukcyjny + HIPEC) wynosi średnio 6-8 godzin.
Z tego też powodu, pomimo obecności zaawansowanej choroby nowotworowej, pacjent musi być w dostatecznie dobrej kondycji fizycznej, aby mógł być poddany długotrwałemu, obciążającemu zabiegowi operacyjnemu, znieść konsekwencje działań anestezjologicznych, chirurgicznych, jak i zastosowania wysokich dawek cytostatyków.
Więcej informacji na temat HIPEC
Leczenie uogólnionego raka żołądka
Paliatywna chemioterapia u chorych na nieoperacyjnego raka żołądka w porównaniu z leczeniem objawowym wydłuża przeżycie i poprawia jego jakość. U części chorych
z granicznie nieresekcyjnymi guzami zastosowanie leczenia systemowego może umożliwić wykonanie resekcji z założeniem radykalności (ponowny zabieg operacyjny po uzyskaniu remisji guza – zmniejszenia stopnia zaawansowania). Wybór schematu terapii powinien opierać się na całościowej ocenie chorego, stanie sprawności oraz profilu działań niepożądanych.
Do schematów chemioterapii o największej skuteczności należy skojarzenie soli platyny (cisplatyna lub oksaliplatyna) z fluoropirymidyną oraz epirubicyną (schematy oznaczane jako ECF, ECX, EOX).
Dodanie docetakselu do schematu zawierającego FU i cisplatynę (DCF) wpływa na wydłużenie czasu przeżycia w porównaniu z terapią wyłącznie 2. lekową, ale wiąże się
z większą toksycznością.
Szczególną uwagę należy zwrócić na ochronę szpiku kostnego, jako tkanki najbardziej podatnej na toksyczność chemioterapeutyków; stąd też profilaktycznie u niektórych pacjentów należy zastosować preparaty stymulujące szpik (granulopoetyny).
Zastąpienie FU kapecytabiną oraz cisplatyny oksaliplatyną w schemacie ECF nie zmniejsza skuteczności leczenia, natomiast jest lepiej tolerowane przez chorych, nie wymaga dożylnego nawadniania i podawania ciągłych wlewów wymagających centralnego dostępu żylnego. W przypadku chorych z przeciwwskazaniami do podania cisplatyny (uszkodzenie nerek, nadwrażliwość na lek) wykazano porównywalną skuteczność schematu zawierającego irynotekan z FU oraz folinianem wapnia. Monoterapię FU można zastosować z powodzeniem u chorych w gorszym stopniu sprawności, z przeciwwskazaniami do leczenia antracyklinami lub pochodnymi platyny i dużym ryzykiem nietolerancji działań niepożądanych.
W przypadku wykazania w badaniach molekularnych nadekspresji bądź amplifikacji receptora HER2 w komórkach raka, wskazane jest dodanie trastuzumabu do schematu zawierającego cisplatynę i fluoropirymidynę w leczeniu 1 linii.
Trastuzumab jest rekombinowanym humanizowanym przeciwciałem monoklonalnym łączącym się wybiórczo z receptorem ludzkiego naskórkowego czynnika wzrostu typu 2 (Human Growth Factor Receptor – HER2). Trastuzumab ma zdolność specyficznego wiązania się z domeną IV pozakomórkowej części receptora HER2 a blokując go, hamuje nadmierną proliferację komórek guza oraz osłabia proces angiogenezy, czyli tworzenia nowych naczyń włosowatych zaopatrujących guz.
Chemioterapia i radioterapia
Pojęcia onkologiczne:
Chemioterapia uzupełniająca (inaczej chemioterapia adjuwantowa) jest stosowana po wykonaniu zabiegu radykalnego.
Chemioterapia paliatywna jest sposobem leczenia po zabiegu operacyjnym innym niż operacja radykalna.
Chemioterapia indukcyjna to sposób leczenia z zamiarem ograniczenia miejscowego choroby i stworzenia w ten sposób warunków do wykonania zabiegu operacyjnego.
Leczenie systemowe w raku żołądka nie jest standardowe i jest wykonywane w ramach badań klinicznych lub jako leczenie paliatywne. Wpływ na brak standaryzacji leczenia systemowego mają różne wyniki badań różnych schematów chemioterapii, także w połączeniu z radioterapią (radiochemioterapia). Do najczęściej stosowanych leków w chemioterapii żołądka należą: 5-fluorouracyl, cisplatyna, epirubicyna, docetaksel, oksaliplatyna, kapecytabina.
Radiochemioterapia została opisana jako sposób leczenia uzupełniającego, dającego korzystne wyniki przeżyć odległych i ograniczenia częstości wznów miejscowych u chorych, u których nie wykonano w większości rozległego usunięcia regionalnych węzłów chłonnych w zakresie D2, co jest standardem także w Polsce.
Pooperacyjna (adjuwantowa) radiochemioterapia zwiększa odsetek 3-letnich przeżyć całkowitych o 11% w porównaniu z jedynie leczeniem chirurgicznym (mediana przeżycia 36 mies. v. 27 mies.). Jednak żadne leczenie uzupełniające nie jest w stanie poprawić dostatecznie wyników leczenia, jeśli zabieg operacyjny nie był wykonany radykalnie, włącznie z wycięciem regionalnych węzłów chłonnych (limfadenektomia) w zakresie D2.
Leczenie obejmuje 1 kurs chemioterapii złożonej z FU w dawce 425 mg/m2/dobę przez 5 dni i folinianu wapniowego 20 mg/m2/dobę przez 5 dni, następnie po 28 dniach napromienianie do dawki 45 Gy (frakcje 1, 8 Gy) wraz z chemioterapią według schematu: FU 400 mg/m2 wraz z folinianem wapniowym w dawce 20 mg/m2/dobę przez pierwsze 4 i przez 3 ostatnie dni napromieniania, a po miesiącu od zakończenia radioterapii 2 kolejne cykle chemiotoerapii, w dawkach jak w pierwszym kursie, podawane w odstępie miesiąca. Obszar napromieniania powinien obejmować lożę żołądka i regionalne węzły chłonne. Po resekcji R1 wskazane jest podwyższenie dawki na obszar zajętego obszaru do 50–54 Gy.
Radioterapia paliatywna (pacjenci bez możliwości technicznych leczenia radykalnego) jest uzasadniona i stosowana w przypadkach nieresekcyjnego raka żołądka z objawami towarzyszącymi: niedokrwistością oraz zwężeniem bądź niedrożnością w okolicy wpustu lub odźwiernika, o ile tam umiejscowiony był guz.
Zastosowanie napromieniania w dawce 30 Gy, w 10 frakcjach, może na pewien czas (3–6 miesięcy) zmniejszyć krwawienie z guza lub względnie poprawić pasaż treści pokarmowej.
W związku z tym nadal niejasne jest miejsce leczenia chemicznego i radioterapii w leczeniu raka żołądka. Planując radioterapię należy wziąć także pod uwagę powikłania związane z popromiennym uszkodzeniem jelit, co może doprowadzić do zmian zapalnych i powstania wtórnej niedrożności wymagającej interwencji chirurgicznej.
Rokowanie, obserwacja po leczeniu i postępowanie w przypadku nawrotów
Rokowanie zależy od stopnia zaawansowania histologicznego (grade) i klinicznego (klasyfikacja TNM - głębokość i rozległość naciekania guza, obecność przerzutów do węzłów chłonnych, przerzuty do otrzewnej, przerzuty odległe). 60 % chorych z II° zaawansowania klinicznego przeżywa 5 lat, z III° – 30 % przeżywa 5 lat, zaś w przypadku stwierdzenia przerzutów odległych nie więcej niż 5 % chorych przeżywa 5 lat.
Ponad 90 % chorych z rakiem wczesnym, ograniczonym do błony śluzowej i podśluzowej, przeżywa 10 lat, co jest synonimem wyleczenia.
Nie ustalono optymalnego schematu nadzoru po leczeniu. Zwykle zaleca się wizyty kontrolne w przychodni onkologicznej co 3–6 miesięcy przez pierwsze 2 lata od zakończenia leczenia, co 6 miesięcy przez kolejne 3 lata, a później raz w roku. Pacjenci obciążeni rakiem żołądka powinni być szczególnie wrażliwi na jakiekolwiek sygnały mogące sugerować nawrót choroby. Badania obrazowe, endoskopowe oraz badania krwi wykonuje się w zależności od zgłaszanych objawów.
Leczenie nawrotów jest mało skuteczne i w związku z tym wskazania do agresywnego postępowania chirurgicznego są indywidualizowane.
Opracowanie:
lek. med. Paulina Cichon,
Klinika Chirurgii Onkologicznej
Gdański Uniwersytet Medyczny
dr hab. n.med. Tomasz Jastrzębski,
Klinika Chirurgii Onkologicznej
Gdański Uniwersytet Medyczny