
dla pacjentów i lekarzy
Peptyd będący pochodną substancji występującej w mleku matki obiecującym lekiem antynowotworowym
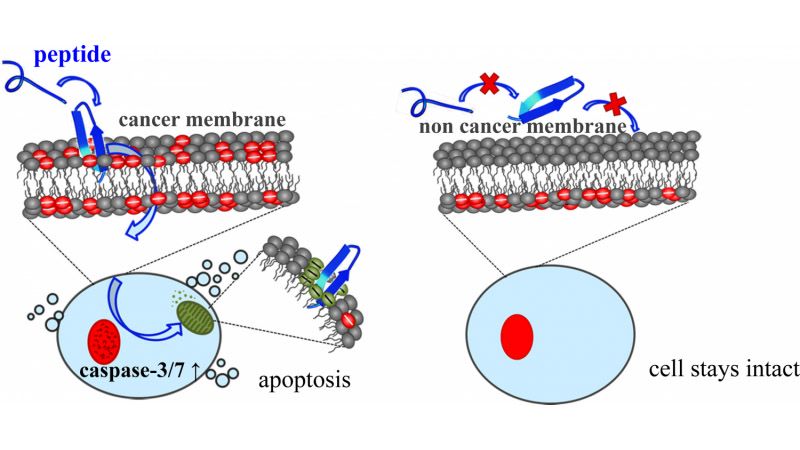
Rys. Peptyd przeciwnowotworowy (niebieski) łączy się z ujemnie naładowanymi markerami PS (czerwone) na zewnętrznej warstwie błony komórki nowotworowej. Peptyd jest wchłaniany do wnętrza komórki nowotworowej, reaguje z mitochondriami (zielony) i indukuje kontrolowane samozniszczenie komórki nowotworowej (apoptoza). Peptyd nie oddziałuje z membraną zdrowych komórek. Źródło: Sabrina Riedl / IMB, Uniwersytet w Graz
Wiele rodzajów nowotworów dobrze reaguje na terapię w przypadku, gdy zmiany zostaną odpowiednio wcześnie wykryte i są leczone za pomocą odpowiedniej chemioterapii. Jednak w przypadku niektórych nowotworów, jak czerniak czy glejak (nowotwór złośliwy mózgu) lub w przypadku odległych przerzutów nowotworowych, leczenie jest trudne i mało efektywne.
Lecz jednak nawet najbardziej złośliwe komórki nowotworowe mają słaby punkt. W przeciwieństwie do zdrowych komórek ludzkiego organizmu, błona komórkowa komórek nowotworowych transportuje na zewnętrzną stronę ujemnie naładowane cząsteczki chemiczne lipidu phosphatidylserine (PS). Cząsteczki lipidu PS znajdujące się na błonie komórkowej komórek nowotworowych mogą służyć jako marker nowotworowy, pozwalając identyfikować zmienione nowotworowo komórki pośród tych zdrowych.
Zespół naukowców z Wydziału Biologii molekularnej Uniwersytetu w Graz (Austria) zidentyfikował i zmodyfikował substancję, która selektywnie trafia w ten właśnie słaby punkt.
We wcześniejszych badaniach zespół z Austrii stwierdził, że marker w postaci lipidu PS dobrze nadaje się jako cel dla opracowania substancji leczniczych ponieważ występuje na powierzchni komórek wielu typów nowotworów.
W dalszej fazie badań naukowcy zajęli się laktoferycyną, peptydem będący pochodną laktoferyny, substancji o działaniu immunomodulującym, przeciwbakteryjnym i przeciwnowotworowym obecnej między innymi w mleku kobiet karmiących.
Zmodyfikowali i wzmocnili aktywną część peptydu. Dodatnio naładowane, zmodyfikowane cząsteczki laktoferycyny lokalizują i dołączają się do ujemnie naładowanych lipidów PS na powierzchni komórki nowotworowej, wnikają do jej wnętrza i w ciągu kilku godzin wywołują śmierć (apoptozę) takiej komórki, nie oddziałując przy tym w żaden sposób na zdrowe komórki organizmu.
Największym wyzwaniem w procesie opracowywania substancji było znalezienie odpowiedniej równowagi pomiędzy toksycznością, a aktywnością. Jeśli peptydy byłyby zbyt aktywne, to atakowałyby również zdrowe komórki. W przeprowadzanych testach zwracano szczególną uwagę by peptydy dołączały się jedynie do komórek nowotworowych.
W latach 2012 – 2016 zespół pracował nad pracował nad najlepszym rozmieszczeniem chemicznych bloków konstrukcyjnych (aminokwasów) aktywnego składnika peptydowego, który ma kształt podobny do spinki do włosów (kształt litery U). Proces projektowania rozpoczęto poprzez symulowanie poziomów aktywności substancji w modelu komputerowym. Potem na tej podstawie zsyntetyzowano około piętnastu najbardziej obiecujących wariantów substancji, a następnie testowano je na modelach membranowych i "in vitro" na liniach komórek nowotworowych.
We współpracy z dr Beate Rinner z Uniwersytetu medycznego w Graz dwa najbardziej obiecujące warianty testowano "in vivo". Naukowcy porównali wyniki leczonych peptydami i nieleczonych myszy, u których wprowadzono ludzkie komórki nowotworowe. U myszy leczonych peptydami badacze zaobserwowali silną lub nawet całkowitą regresję nowotworów, osiągając średnią regresję wynoszącą 85% w przypadku czerniaka i do 50% w przypadku glejaka, w porównaniu do myszy nieleczonych. Zmodyfikowane wersje laktoferycyny wykazały skuteczność około dziesięć razy większą niż laktoferyna obecna w mleku kobiet karmiących.
Aktywne wersje peptydu wykazujące działanie antynowotworowe są obecnie w toku procedury patentowej w Unii Europejskiej i USA. Zespół badaczy współpracuje teraz z firmą farmaceutyczną, w ramach projektu finansowanego przez austriacką rządową agencję (FFG) wspierającą badania naukowe, w celu przygotowania badań przedklinicznych. Nowy środek przeciwnowotworowy powinien być podawany dożylnie, tak aby dotrzeć również do ewentualnych przerzutów. Aktualny etap badań dotyczy stabilności peptydu w układzie krwionośnym, badania czy może przekroczyć barierę krew-mózg oraz zwiększenia skuteczności.
Źródło:
- Sabrina Riedl et al. Human lactoferricin derived di-peptides deploying loop structures induce apoptosis specifically in cancer cells through targeting membranous phosphatidylserine, Biochimica et Biophysica Acta (BBA) - Biomembranes (2015). DOI: 10.1016/j.bbamem.2015.07.018
- Sabrina Riedl et al. Killing of melanoma cells and their metastases by human lactoferricin derivatives requires interaction with the cancer marker phosphatidylserine, BioMetals (2014). DOI: 10.1007/s10534-014-9749-0
- Breast milk as a weapon against cancer, medicalxpress.com